5月1号更新:FDA刚刚批准了瑞德西韦紧急使用授权 (EUA)。疗程分为5天或者10天:已经上了呼吸机的病人,建议10天用药,其他5天。吉利德已经宣布,现有存货全部捐赠,一分钱不收,总共150万剂,大约能治疗14万病人。股票今天下跌4.8%。良心公司啊,吉利德为了这个药,今年已经花了5000万美元用于生产和临床试验,预计全年要花费10亿美元。
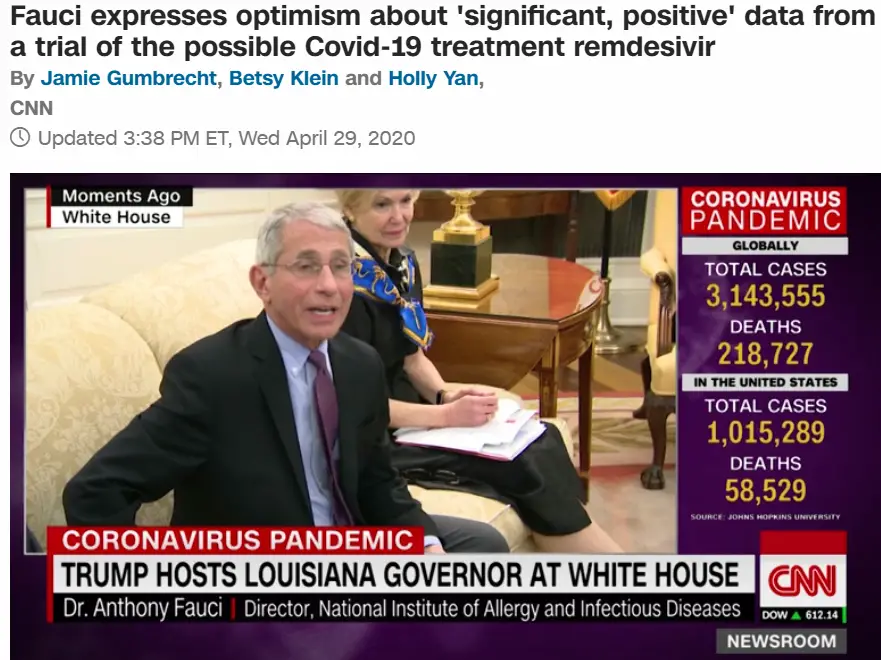
一波三折,吉利德的瑞德西韦(“人民的希望”)终于盼来了好消息,全球第一个大型双盲三期临床试验结果出炉:有效!
这是美国过敏与传染病研究所主导的临床,全球收治了1090个病人,随机,双盲,安慰剂对照一应俱全。
这个研究所的所长就是大名鼎鼎的Dr. Fauci,一贯发言非常谨慎,但是这次毫不犹豫:
”数据表明瑞德西韦能明确地,显著地缩短治愈时间“ (”The data shows that remdesivir has a clear-cut, significant, positive effect in diminishing the time to recovery.”)
早期结果表明治愈时间从15天缩短到11天。Fauci说虽然31%听起来并不是100%立竿见影,但是这是一个很重要的证据,说明瑞德西韦能有效抑制病毒。
一般情况下早期临床结果不会这么快公布,但是Fauci说这么做的目的是让对照组里服用安慰剂的患者尽早改用真正的药品,否则不人道。
纽约时报报道FDA正在考虑紧急授权,最快今天就能批准。
注意紧急授权(EUA)不是常规FDA批准,但是授权之后,更多病人就可以使用瑞德西韦治病了,目前只有少量同情用药和临床试验。
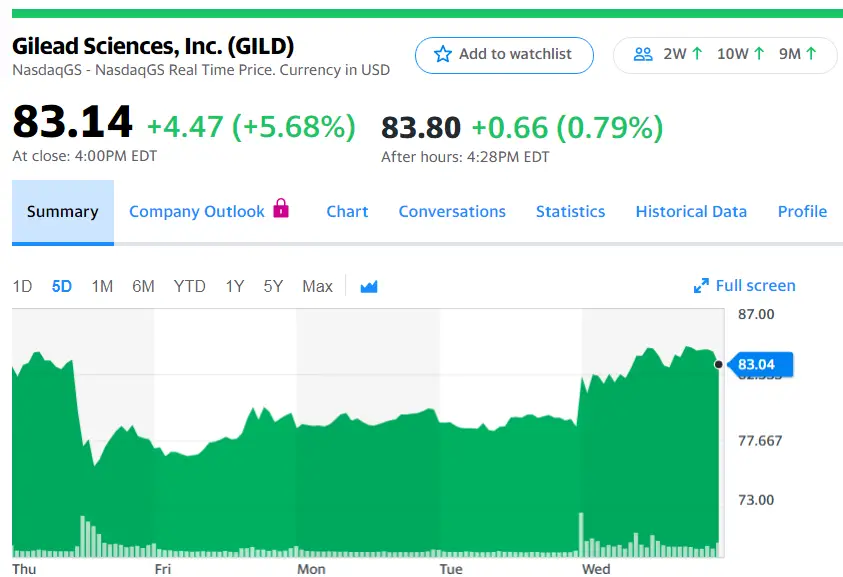
吉利德股票今天涨了5.68%
同在今天,曹彬教授的文章也在柳叶刀发表了:“本试验发现,尽管瑞德西韦安全、耐受性好,但与安慰剂相比并没有显著的益处“。
但是中国的临床试验规模小了很多,只有237名病人,而且没有做完就提前终止了。
所以从投资者的反应来看,显然更相信美国传染病研究所1000多人的试验。
WHO今天也泼了一桶冷水,说一个试验往往不能证明效果,现在就认定瑞德西韦有效为时过早。
理论上讲也是对的,只是疫情之下,等不得六个月。
其实也好办,相信中国和WHO的,别用瑞德西韦。
相信美国的,尽管用。
除了传染病研究所以外,还有多个临床试验在全球同时开展。
早先有一个小型的重症试验,397个病人,结果也非常好,但是没有对照组。
这个试验的关键点是重症。因为病毒在体内大面积扩散之后,药物能起到的作用越来越小,何况很多是老年人和有基础病的人,等到多个器官受损,往往就回天无力了。所以重症试验更有说服力。
不久前芝加哥大学透露出来的信息是瑞德西韦对重症效果显著,而且5天疗程和10天疗程差不多。详见:
- 重症6天出院!芝加哥大学:瑞德西韦效果显著(2020-04-06)
还有更早的文章:
- 吉利德CEO首次回应专利问题:患者第一! (2020-02-05)
- 世卫组织:瑞德西韦是目前唯一可能有效的药物(2020-02-24)
- 满载地球人希望的 remdesivir (2020-01-31)
虽然现在还不能断言瑞德西韦一定对治疗新冠病毒有效,但是今天的消息还是非常振奋人心的。希望更多的患者,如果自己愿意,能够尽早试用。另外很有可能一款药对某些病人有效,对其他人效果不明显,这也是很正常的。或许将来会有多种药品都有一定程度的疗效,包括瑞德西韦,包括氯喹,还有正在研发的新药。
随着更多临床结果出炉,相信医学界会有一个更全面的认识。从目前有限的数据来看,三个临床试验,两个美国的证明有效,一个中国的证明无效。